Andrew Cassy aveva trascorso la sua vita lavorativa in un dipartimento di ricerca sulle telecomunicazioni fino a quando una diagnosi di morbo di Parkinson nel 2010 lo spinse al pensionamento anticipato. Incuriosito dalla sua malattia, che considerava un problema di ingegneria, decise di offrirsi volontario per gli studi clinici.
“Avevo tempo, qualcosa di prezioso che potevo dare al processo di comprensione della malattia e di ricerca di buoni trattamenti”, dice.
Nel 2024 è stato accettato in un processo radicale. Quell’ottobre, i chirurghi di Lund, in Svezia, inserirono nel suo cervello neuroni derivati da cellule staminali embrionali umane (ES). La speranza è che alla fine possano sostituire parte del tessuto danneggiato.

Le cellule staminali invertono il diabete femminile: una novità mondiale
Lo studio è uno degli oltre 100 studi clinici che esplorano il potenziale delle cellule staminali per sostituire o integrare i tessuti in malattie debilitanti o pericolose per la vita, tra cui cancro, diabete, epilessia, insufficienza cardiaca e alcune malattie degli occhi. Si tratta di un approccio diverso dalle terapie non approvate spacciate da molte cliniche losche, che utilizzano tipi di cellule staminali che non si trasformano in nuovi tessuti.
Tutte le prove sono piccole e si concentrano principalmente sulla sicurezza. E ci sono ancora sfide sostanziali, tra cui definire quali cellule saranno più adatte per quali scopi e capire come aggirare la necessità di farmaci immunosoppressori che impediscono al corpo di respingere le cellule ma aumentano il rischio di infezioni.
Tuttavia, la raffica di studi clinici segna un punto di svolta per le terapie con cellule staminali. Dopo decenni di intensa ricerca che a volte ha innescato controversie etiche e politiche, la sicurezza e il potenziale delle cellule staminali per la rigenerazione dei tessuti vengono ora ampiamente testati. “Il ritmo dei progressi è stato notevole”, afferma lo specialista in cellule staminali Martin Pera del Jackson Laboratory di Bar Harbor, nel Maine. “Sono passati solo 26 anni da quando abbiamo imparato per la prima volta a coltivare le cellule staminali umane in fiasche.”
I ricercatori si aspettano che alcune terapie con cellule staminali entrino presto in campo clinico. I trattamenti per alcune patologie, dicono, potrebbero diventare parte della medicina generale tra cinque o dieci anni.
Trovare una fonte
I sintomi di Cassy sono iniziati con un piccolo e persistente tremore alle dita quando aveva appena 44 anni. I sintomi motori caratteristici del Parkinson sono guidati dalla degenerazione dei neuroni che producono dopamina chiamati cellule A9 nella substantia nigra del cervello. I farmaci che sostituiscono la dopamina mancante sono efficaci, ma hanno effetti collaterali tra cui movimenti incontrollati e comportamenti impulsivi. E man mano che la malattia progredisce, l’efficacia dei farmaci diminuisce e gli effetti collaterali peggiorano.
L’idea di sostituire le cellule dopaminergiche degenerate ha una lunga storia. Durante lo sviluppo, le cellule ES pluripotenti, che hanno il potenziale per diventare molti tipi cellulari, si trasformano in cellule specializzate del cervello, del cuore, dei polmoni e così via. Teoricamente, le cellule staminali trapiantate potrebbero riparare qualsiasi tessuto danneggiato.
Il Parkinson si prestava a testare questa teoria. Il primo trapianto di tali cellule ebbe luogo in Svezia nel 1987 utilizzando neuroni provenienti dal cervello in via di sviluppo di feti di gravidanze interrotte, all’epoca l’unica fonte di cellule neurali immature, o progenitrici. Da allora, più di 400 persone affette da Parkinson hanno ricevuto un trapianto di questo tipo, con risultati contrastanti. Molte persone non hanno riscontrato alcun beneficio o hanno avuto effetti collaterali debilitanti. Ma altri sono migliorati così tanto che non hanno più avuto bisogno di assumere farmaci dopaminergici.
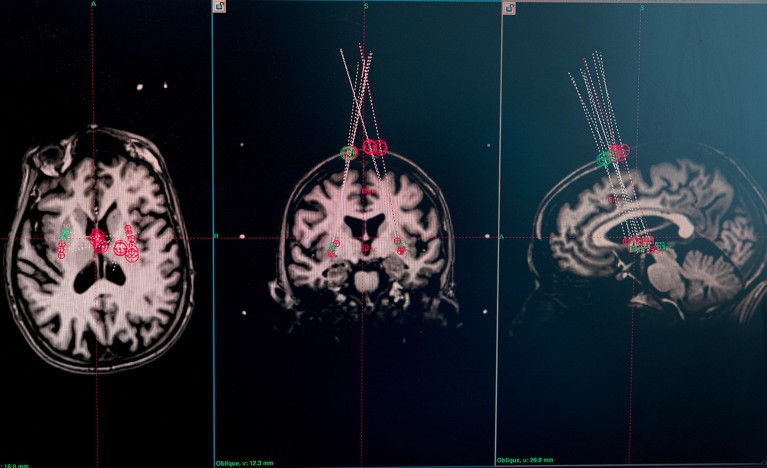
Le scansioni MRI del cervello di un partecipante allo studio vengono utilizzate per pianificare dove l’ago rilascerà le cellule.Credito: Åsa Sjöström per Natura
“Nel complesso, gli studi ci hanno dimostrato che l’approccio può funzionare, a volte in modo trasformativo”, afferma il neurologo Roger Barker dell’Università di Cambridge, nel Regno Unito. “Ma avevamo bisogno di un materiale di partenza più affidabile.”
Il tessuto cerebrale fetale non può essere standardizzato e potrebbe anche essere contaminato da progenitori destinati a maturare nel tipo sbagliato di cellule. Oltre a ciò, alcune persone hanno obiezioni etiche o religiose all’uso di questo materiale. E in ogni caso, nota Barker, spesso è stato difficile trovare materiale sufficiente per procedere a un’operazione di trapianto delle cellule.
Le prospettive per la terapia rigenerativa con cellule staminali sono migliorate quando è diventato possibile derivare cellule specializzate da fonti più controllabili, in particolare cellule ES umane e, successivamente, cellule staminali pluripotenti indotte (iPS), che vengono create riprogrammando le cellule adulte per tornare a uno stato immaturo . Oggi è possibile produrre in modo affidabile un gran numero di cellule specializzate con una qualità e una purezza sufficientemente elevate per la clinica.
La ricercatrice sulle cellule staminali Agnete Kirkeby dell’Università di Copenaghen e i suoi colleghi hanno esaminato il panorama degli studi clinici sulle cellule staminali rigenerative in tutto il mondo e, a dicembre 2024, hanno identificato 116 studi approvati o completati su una serie di malattie1. Circa la metà utilizza cellule ES umane come materiale di partenza. Gli altri studi utilizzano cellule iPS, disponibili in commercio o generate da cellule della pelle o sangue di singole persone per trattare le proprie condizioni. Dodici degli studi tentano di trattare la malattia di Parkinson utilizzando cellule produttrici di dopamina derivate da cellule staminali.
Promessa per il Parkinson
Lo studio a cui è iscritta Cassy, di cui Barker è co-conduttore, e un altro studio più avanzato condotto da BlueRock Therapeutics, una società di biotecnologie con sede a Cambridge, Massachusetts, ha dato ai partecipanti cellule progenitrici A9 derivate da cellule ES umane. Lo studio BlueRock ha riportato i risultati preliminari per i suoi 12 partecipanti. Due anni dopo, il trattamento si è dimostrato sicuro e ha mostrato segni di efficacia in coloro che hanno ricevuto la dose più alta tra le due. Finora, nessuno studio sul Parkinson ha riportato effetti collaterali legati al movimento incontrollato, come quelli osservati con i farmaci dopaminergici e in alcuni studi che hanno utilizzato tessuto fetale.

La corsa per potenziare le cellule T che combattono il cancro
Rispetto ad altri organi, come cuore, pancreas e reni, il cervello si è rivelato uno degli organi più semplici da trattare con le cellule staminali. Un vantaggio è che il cervello è ampiamente protetto dal sistema immunitario del corpo, che cerca e distrugge i tessuti estranei. I partecipanti agli studi sul Parkinson ricevono immunosoppressori solo per un anno per coprire il periodo in cui la barriera ematoencefalica guarisce dall’intervento chirurgico. I partecipanti agli studi su altri organi in genere ricevono i farmaci per il resto della loro vita.
E il cervello è accomodante. Le cellule A9 di solito risiedono nella substantia nigra e inviano proiezioni al putamen, nel prosencefalo, dove rilasciano dopamina. Ma i neurochirurghi spesso inseriscono le cellule progenitrici direttamente nel putamen perché è più facile da raggiungere chirurgicamente. La capacità del cervello di adattarsi al tessuto fetale e alle cellule trapiantate nel sito “sbagliato” è “piuttosto intelligente”, afferma Barker.
Altrettanto notevole, dice, è uno studio sull’epilessia in cui cellule trapiantate derivate da cellule ES umane si integrano nei circuiti neurali corretti nel cervello. Nello studio clinico, condotto dalla società di biotecnologie Neurona Therapeutics con sede a San Francisco, in California, i chirurghi hanno trapiantato versioni immature di un tipo di cellule cerebrali chiamate interneuroni nel cervello di dieci persone affette da una forma di epilessia che non poteva essere controllata dai farmaci. Prima di ricevere questo trattamento, le crisi epilettiche dei partecipanti erano così frequenti e debilitanti che non potevano vivere in modo indipendente.

Un cervello di ratto con cellule derivate da cellule staminali trapiantate viene messo nel ghiaccio e tagliato a fette in preparazione per l’analisi. Queste cellule sono state testate sui ratti prima che fosse approvato uno studio clinico in corso su persone affette da malattia di Parkinson.Credito: Åsa Sjöström per Natura
Un anno dopo il trapianto, la frequenza delle crisi epilettiche gravi nei primi due partecipanti era scesa quasi a zero, un effetto che si è mantenuto per due anni. La maggior parte degli altri partecipanti ha avuto una marcata riduzione della frequenza delle crisi. Non ci sono stati effetti collaterali significativi e nessun danno cognitivo, riferisce la società. Lo scorso giugno, la Food and Drug Administration statunitense ha concesso alla terapia lo status di “fast track” per accelerare il processo che porta all’approvazione normativa.
“I risultati per i pazienti sono stati sorprendentemente simili anche se le procedure sono state eseguite in diversi siti in tutto il paese”, afferma Arnold Kriegstein dell’Università della California, a San Francisco, co-fondatore di Neurona Therapeutics. “È molto robusto.”
Come il cervello, l’occhio è ben protetto dal sistema immunitario del corpo. Kirkeby e i suoi colleghi hanno identificato 29 studi clinici per le malattie oculari, in particolare per i tipi di degenerazione maculare legata all’età. Altri organi non hanno lo stesso privilegio immunitario, ma sono responsabili di alcune delle malattie più gravi, tra cui l’insufficienza cardiaca e il diabete di tipo 1, causato dalla distruzione delle cellule delle isole produttrici di insulina nel pancreas.
Oltre il cervello e gli occhi
I progressi sono stati più lenti per altre condizioni. Ma i primi risultati positivi di uno studio condotto dalla società farmaceutica Vertex Pharmaceuticals con sede a Boston, Massachusetts, hanno generato un’ondata di ottimismo per il diabete. Il biologo specializzato in cellule staminali Douglas Melton e i suoi colleghi hanno sviluppato le prime cellule insulari funzionali da una linea cellulare ES umana nel 2014 presso l’Università di Harvard a Cambridge2. Ora presso Vertex, sta conducendo una sperimentazione su persone affette da forme particolarmente gravi della malattia, utilizzando cellule insulari proprietarie generate con metodi simili. Le cellule svolgono il loro lavoro ovunque si trovino nel corpo, in questo caso nel fegato. Secondo l’azienda, 9 dei 12 partecipanti che hanno ricevuto la dose intera non hanno più avuto bisogno di iniettare insulina e altri due hanno potuto ridurre la dose.
“Sono rimasto sorpreso e felice che abbia funzionato così bene”, afferma Melton, che si è trasferito in questo campo negli anni ’90, quando a suo figlio è stato diagnosticato il diabete di tipo 1. “E sono particolarmente felice di vedere il potenziale che ha per i pazienti.”
Il laboratorio di Malin Parmar presso l’Università di Lund, in Svezia, ha sviluppato cellule sostitutive derivate da cellule staminali per uno studio in corso che sta tentando di utilizzare la terapia con cellule staminali per sostituire il tessuto danneggiato nelle persone affette da malattia di Parkinson.Credito: Åsa Sjöström per Natura
Il cuore si è rivelato particolarmente fastidioso per la medicina rigenerativa. È una pompa grande e complessa composta da diversi tipi di cellule e qualsiasi danno deve essere riparato In situ. Christine Mummery, scienziata specializzata in cellule staminali presso l’Università di Leiden nei Paesi Bassi, è stata una delle prime a generare cellule muscolari cardiache battenti3o cardiomiociti, da cellule ES umane nel 2002. Ma si rese presto conto di quanto sarebbe stato difficile portarli in clinica, in particolare quando vide un cuore grasso e profondamente sfregiato rimosso durante un intervento di trapianto. “Ho pensato: non saremo in grado di risolverlo presto.” Ha cambiato la sua direzione di ricerca verso la modellazione delle malattie. Ma con circa 64 milioni di persone in tutto il mondo affette da insufficienza cardiaca, Mummery afferma di apprezzare la tenacia di coloro che non si sono arresi.



